Некоторые ошибки диагностики бронхиальной астмы
В.К. Трескунов, И.В. Сидоренко, Т.В. Захаржевская, Н.А. Дидковский
Резюме
Статья посвящена актуальной проблеме медицины – трудностям диагностики бронхиальной астмы. Авторы исследуют причины как гипо - так и гипердиагностики заболевания. Подчеркивается значение тщательно собранного анамнеза, исследования функции внешнего дыхания и фармакологических проб в решении диагностических задач.
Как правило, при заболевании органов дыхания побудительным симптомом, заставляющим больного обратиться к врачу, является возникновение дыхательного дискомфорта (диспноэ). Дальнейшая судьба больного будет зависеть от правильно поставленного диагноза(1). Первым заболеванием, которое находится в списке возможных причин одышки, по-видимому, будет бронхиальная астма.
По определению экспертов ВОЗ, бронхиальная астма — «хроническое заболевание, основой которого является воспалительный процесс в дыхательных путях с участием разнообразных клеточных элементов, включая тучные клетки, эозинофилы и Т-лимфоциты. У предрасположенных к бронхиальной астме лиц этот процесс приводит к развитию генерализованной бронхиальной обструкции различной степени выраженности, полностью или частично обратимой спонтанно или под влиянием лечения» (2). Воспалительный процесс вызывает усиление ответа дыхательных путей в виде бронхоспазма на различные внешние и внутренние стимулы. Под это определение попадают от 4 до 10 процентов больных, страдающих заболеваниями органов дыхания(3). Поэтому можно сказать, что бронхиальная астма является одним из самых распространенных заболеваний органов дыхания, как у взрослых, так и у детей (4). По экспертной оценке академика А.Г. Чучалина в России бронхиальной астмой страдают около 7 миллионов человек(1), причем истинное число больных превышает число диагностированных случаев в 1,5 – 6 раз (5). Заболевание обычно протекает длительно с периодическими обострениями, снижая качество жизни, приводя больного к инвалидности и, иногда, к гибели. На поддержание стабильного течения бронхиальной астмы и удовлетворительного качества жизни больного уходят значительные материальные ресурсы.
К сожалению, несмотря на многовековое пристальное внимание медицинской общественности к решению проблем бронхиальной астмы, заболевание остается до сих пор во многом неизученным. Часто перед практикующим врачом возникают диагностические проблемы, так как отсутствует четкое представление о центральном звене патогенеза заболевания, что отражает и определение, данное комитетом экспертов. Поэтому в диагностике бронхиальной астмы врач, как правило, руководствуется древнегреческим выражением: ἆσθμα — «тяжелое дыхание, одышка», что порождает многочисленные ошибки, которые способны в корне изменить ход лечения и прогноз заболевания.
В клинической практике встречаются проявления как гиподиагностики, так и гипердиагностики бронхиальной астмы. Попытаемся выделить основные нозологические единицы, которые по своей клинической картине похожи на бронхиальную астму и могут стать причиной диагностической ошибки.
Примеры гиподиагности бронхиальной астмы
Гиподиагностика заболевания - это ситуация, когда под влиянием объективных и субъективных обстоятельств врач вместо бронхиальной астмы распознает у больного другую, схожую по клинической картине болезнь. Этому способствуют несколько причин.
Первая причина: не проводится объективное исследование механизма одышки. Больного просто не направили на исследование функции внешнего дыхания (ФВД) или направили, но полученная при этом кривая «поток-объем» форсированного выдоха имеет нормальную конфигурацию. Надо учитывать, что даже если при базисном исследовании получены параметры, не выходящие за рамки расчетной нормы, нельзя полностью исключить наличие у больного какого-либо обструктивного заболевания легких. Всегда надо иметь в виду, что существующие на сегодняшний день таблицы расчета должных величин не дают 100% гарантии точности оценки в каждом конкретном случае. К тому же, даже при нормальных значениях объема форсированного выдоха за первую секунду (ОФВ1) ингаляция β2-агониста может выявить у больного скрытый бронхоспазм. Отсюда вытекает вторая причина гиподиагностики бронхиальной астмы.
Причина вторая: после получения данных о нарушении бронхиальной проходимости больному не проводится фармакологическая проба на обратимость обструкции.
Рассмотрим некоторые заболевания и патологические синдромы, которые нередко маскируют бронхиальную астму при недостаточно полном исследовании ФВД.
При анализе амбулаторных карт многих поликлиник города Москвы, можно нередко встретить диагноз: «Хронический обструктивный бронхит». Иногда этот грозный диагноз принадлежит пациенту, порой молодого возраста, который периодически, чаще на фоне вирусной инфекции верхних дыхательных путей, начинает задыхаться, синеть, у него в легких выслушиваются сухие свистящие хрипы. После купирования воспалительных явлений верхних дыхательных путей длительно беспокоят: приступообразный кашель, отделение мокроты, одышка, а также проявления неспецифической трахеобронхиальной гиперреактивности. Например, у данного больного в холодную ветреную погоду при выходе из теплого помещения на улицу возникают: приступообразный кашель, одышка, свистящее дыхание. Подобные симптомы появляются при глубоком вдохе, смехе или физической нагрузке. При тщательном расспросе больного можно услышать, что при контакте с животными, домашней пылью, пыльцой растений, иногда после приема аспирина появляются клинические симптомы нарушения дыхания, чихание и раздражение слизистой глаз. Первый же анализ крови выявляет эозинофилию. Мокрота при осмотре желтого цвета, под микроскопом – в мазке находят множество кристаллов Шарко-Лейдена и эозинофилов.
Иногда проходят годы пока, наконец, врач не попытается купировать «приступ одышки» ингаляцией β2-агониста и, когда на глазах у всех произойдет «чудесное» исцеление, диагноз «обструктивного бронхита» трансформируется в бронхиальную астму с соответствующей терапией и прогнозом.
Причина третья: при достаточно яркой клинической картине бронхиальной астмы проба с β2-агонистом β2-агонистом не выявляет обратимость обструкции дыхательных путей.
Рассмотрим следующую ситуацию: пациенту с диагнозом «хронический обструктивный бронхит» проводится исследование функции внешнего дыхания. При анализе кривой «поток-объем» выявляется снижение потока выдыхаемого воздуха. Следующий, обязательный для функционального диагноста шаг – проведение пробы с β2-агонистом. Если через 15-30 минут после вдыхания через спейсер 400 мкг албутерола получается достоверный прирост бронхиальной проходимости: увеличение на 200 мл ОФВ1 - 12% и более от исходного значения ОФВ1, диагноз бронхиальной астмы подтверждается. Такая ситуация наблюдается далеко не всегда, В ряде случаев, после пробы с β2-агонистом врач не получает достоверного прироста ОФВ1 – полученная после ингаляции албутерола обратимость не полная, прирост ОФВ1 не достиг 12% и 200 мл. Такая реакция на прием бронхолитического средства может означать, что ведущим механизмом бронхообструкции в данном случае является воспалительный отек слизистой бронхов у этого пациента. Если пациенту повторить пробу на обратимость после семидневного приема 30 мг преднизолона внутрь, отек слизистой бронхов уменьшится и гладкая мускулатура обретет способность к бронходилятации. Прирост ОФВ1 теперь может достигнуть 12% и 200 мл и более.
Причина четвертая: длительная ремиссия бронхиальной астмы часто наводит врача на мысль об ошибочности диагноза, так как симптомы заболевания и снижение показателей кривой «поток-объем» форсированного выдоха при исследовании ФВД отсутствуют. В данной ситуации необходимо помнить о врожденной способности гладкой мускулатуры бронхов больного бронхиальной астмой реагировать бронхоспазмом при специфическом и неспецифическом контакте с различными бронхоконстрикторами (аллергены, медиаторы аллергических реакций, изменение осмомолярности секрета бронхов и так далее). В основе избыточной готовности гладкой мускулатуры бронхов больных бронхиальной астмой находятся феномены: трахеобронхиальная гиперрективность (ТБГР) и гиперчувствительность (ТБГЧ), которые на ряду с обратимостью бронхиальной обструкции, рассматриваются как патогенетическая основа клинический картины бронхиальной астмы. ТБГР и ТБГЧ могут существовать у больного длительное время скрыто и проявляться под влиянием воздействия вирусной инфекции, аллергической реакции или нервного стресса.
Под трахеобронхиальной гиперреактивностью понимают: значительное падение показателей кривой «поток-объем» форсированного выдоха в ответ на контакт с бронхоконстрикторами, не вызывающими подобную реакцию у человека, не страдающего бронхиальной астмой, например, гипервентиляция, метахолин, гистамин, аденозин. Правда, в литературе представлены случаи обнаружения трахеобронхиальной гиперреактивности у пациентов с аллергическим ринитом(6), муковисцидозом (7) и хроническим бронхитом (8). Этот факт не уменьшает диагностического значение ТБГР в патогенезе бронхиальной астмы. Практикующему врачу хорошо известно, что аллергический ринит нередко предшествует появлению приступов удушья. В медицинской практике иногда трудно четко разграничить хронический обструктивный бронхит с бронхиальной астмой.
При муковисцидозе можно предположить наличие у больного ТБГР, так у некоторых больных с кистозным фиброзом находят поливалентную сеснсибилизацию к экзоаллергенам, которая может привести к гиперреактивности воздухоносных путей.
Трахеобронхиальная гиперчувствительность – это способность дыхательных путей отвечать бронхоспазмом на минимальные количества вещества, совершенно безобидного для лиц, не страдающих бронхиальной астмой. Вместе, гиперчувствительность и гиперреактивность, по-видимому, составляют основу патогенеза бронхиальной астмы.
Кроме наследуемых факторов формированию ТБГР и ТБГЧ способствует хроническое воспаление слизистой дыхательных путей. Не имеет значения, чем вызван воспалительный процесс – воздействием окисляющих полютантов или аллергенов. При рецидивирующем воспалении – к бронхоспазму, при персистирующем поражении – к стойкому нарушению бронхиальной проходимости. Длительный воспалительный процесс приводит к ремоделированию бронхов и потере способности гладкой мускулатуры к бронхоспазму даже, если изначально эта способность имелась. Поэтому больные с ХОБЛ не реагируют бронхоспазмом на ингаляцию гистамина или β -адреноблокатора, в то же время, у больного бронхиальной астмой после контакта с микроскопическим количеством гистамина неизбежно резко падают показатели кривой «поток-объем» форсированного выдоха.
Особенно важно определить наличие трахеобронхиальной гиперреактивности и гиперчувствительности у детей и подростков, так как возникнув в раннем детстве, симптомы бронхиальной астмы у 50% больных стихают в пубертатный период, но это не означает избавления от болезни, ибо остается патогенетическая основа болезни – ТБГР и ТБГЧ. Приступы удушья в любую минуту могут возобновиться под воздействием дополнительных факторов. Например, вирусная инфекция верхних дыхательных путей, интенсивное воздействие аллергена или нервное перенапряжение – все это может стать пусковым механизмом тяжелого рецидива бронхиальной астмы. Только осуществление нескольких бронхоконстрикторных проб (метахолиновый, гистаминовый или с физической нагрузкой тестов), гарантирует при отсутствии клинических и функциональных признаков бронхиальной обструкции от гиподиагностики бронхиальной астмы в период ее стойкой ремиссии.
У больных преклонного возраста, гиподиагностика бронхиальной астмы при наличие кашля и одышки происходит с уклоном в сторону диагноза сердечной недостаточности. Если перед врачом стоит диагностическая задача – определить причину одышки у пожилого пациента, особенно, когда он страдает избыточным весом или перенес инфаркт миокарда, то неизбежно доктор склоняется к мысли о сердечно-сосудистой причине заболевания. При отсутствии попытки дифференцировать происхождение одышки, дальнейшая терапия может усугубить течение заболевания. Хорошо, если больному будут рекомендованы нитраты, которые способны не только усилить коронарный кровоток, но и снизить давление в малом круге кровообращения и снять гипертонус мускулатуры бронхов, и поэтому эффективны при обеих патологиях. Прием больным даже селективного β – адреноблокатора при латентной бронхиальной астме способен резко обострить течение заболевания, спровоцировать тяжелый бронхоспазм. В этой связи, наличие у больного артериальной гипертензии не должено рассматриваться как решающий фактор в дифференциальной диагностике причин одышки у больного. Нередко, обусловленная бронхообструкцией гипертония немедленно купируется у больного бронхиальной астмой после ингаляции β2-агониста. В своей практике каждый терапевт может наблюдать, как после приема β2-агониста у больного с бронхоспазмом уряжается пульс, восстанавливаются нормальные параметры не только дыхательной, но и сердечнососудистой систем.
Уже первый взгляд на задыхающегося пациента позволяет врачу различить сердечнососудистую одышку от бронхоспазма. Как правило, больной с сердечной астмой или отеком легких – бледен, выражен акроцианоз. Он тихо покашливает, сплевывая пенистую, прозрачную мокроту, иногда окрашенную примесью крови. В легких при этом выслушиваются сухие хрипы, но чаще – разнокалиберные влажные над нижними полями грудной клетки. В тяжелом состоянии больного невозможно провести исследование ФВД, тем более пробу на обратимость или трахеобронхиальную гиперреактивность. В этом случае врач должен опираться на данные анамнеза, осмотра, аускультации и реакции больного на терапию.
Если у больного нет острого приступа удушья, можно провести исследование ФВД с помощью пикфлоуметра и определить причину заболевания. Для этого проще всего попросить пациента резко выдохнуть в прибор столько раз, сколько нужно, чтобы получить стабильные результаты. Получив низкие цифры мощности форсированного выдоха, необходимо провести пробу на обратимость обструкции. Если достоверный, 10% и более, прирост мощности форсированного выдоха не получен, тогда рекомендуется ежедневное, 2 раза в сутки проведение пикфлоуметрии в течение недели и, если разброс показателей утро-вечер будет превышать 10%, диагноз бронхиальной астмы станет достоверным.
Назначение курса преднизолона (30 мг/сутки в течение 7 дней) делает пробу еще более эффективной. Снижение уровня отека бронхиального дерева под влиянием глюкокортикостероида у больного бронхиальной астмой отразится в виде неуклонного возрастания показателя пикфлоуметрии. Диагностические возможности врача возрастают при использовании исследования ФВД с помощью автоматического спироанализотора с применением фармакологической пробы с β2-агонистом.
Очень часто причиной гиподиагностики бронхиальной астмы у взрослых является увлечение диагнозом ХОБЛ. Врачу необходимо помнить, что пока данная нозология представляет собой значительные трудности для лечения и имеет фатальный прогноз. Развивается ХОБЛ исподволь, длительное воздействие на слизистую воздухоносных путей окислителей, содержащихся в табаке, аллергенов, медиаторов воспаления у предрасположенных людей к 40 годам формирует стойкую, неуклонно развивающуюся обструкцию трахеобронхиального дерева с соответствующей клинической картиной. С бронхиальной астмой ХОБЛ объединяют наличие хронического воспаления слизистой воздухоносных путей и их обструкции, но при бронхиальной астме имеется возможность с помощью адекватной фармакотерапии остановить нарастание бронхиальной обструкции, нередко купировать воспаление в бронхах, а при ХОБЛ лечение заболевания представляет пока существенные трудности и недостаточно эффективно.
Мы провели обследование 48 больных с диагнозом ХОБЛ, который был выставлен в одном из пульмонологических стационаров города Москвы. Из всей группы обследованных пациентов, только 3 удалось сохранить ранее поставленный диагноз. В остальных случаях диагноз ХОБЛ был снят, так как при функциональном обследовании пациенты не только показывали более 12% обратимости обструкции, но и соотношение ОФВ1 к ФЖЕЛ оказалось более 0,7. К тому же, примерно трети пациентам диагноз ХОБЛ ставился, когда они еще не преодолели 35 летний рубеж.
Необходимо отметить, что при проведении исследования ФВД оценка полученных результатов возможна только при соблюдении существующих правил: отсутствие замедленного старта, наличие достаточного усилия при выдохе, а также продолжение форсированного выдоха не менее чем в течение 6 секунд. Общепринятым минимумом количества маневров, пригодных для оценки - это 3 попытки. Результаты 2 из них должны быть сопоставимы, то есть максимальное значение ОФВ1 и ФЖЕЛ отличается от второго по величине – не более чем на 150 мл (5%), критерии ATS/ERS-2005 (10). При правильном проведении маневра во время форсированного выдоха кривая поток-объем не должна содержать признаков дополнительных вдохов, а также кашля или раннего закрытия дыхательных путей. Только в этом случае мы застрахованы от ошибок при оценке степени бронхиальной обструкции. Если выдох продолжается менее 6 секунд, правильное вычисление соотношения ОФВ1 к ФЖЕЛ невозможно, а этот параметр имеет решающее значение в диагностике ХОБЛ. Показатели соотношения ОФВ1 к ФЖЕЛ при ХОБЛ должны быть ≤ 0.70, а ОФВ1 – менее 80%. Берется значение показателей после ингаляции β2-агониста (11). Поэтому проба на обратимость обструкции является обязательным атрибутом стандартного исследования ФВД у больных с одышкой и кашлем.
Примеры гипердиагностики бронхиальной астмы
Проблема гипердиагностики бронхиальной астмы также актуальна, как и проблема гиподиагностики. Причина данного явления кроется, во-первых, в преувеличении значения жалоб больного на кашель и одышку для постановки диагноза бронхиальная астма. Во-вторых, ориентировка врача только на данные базисного исследования ФВД без использования фармакологических проб с β2-агонистом и бронхоконстрикторами может привести врача к неверному диагностическому решению.
Круг заболеваний, скрывающихся под диагнозом бронхиальная астма, достаточно обширен. В литературе описаны хорошо известные практическому врачу случаи, когда больных коклюшем пытаются лечить от бронхиальной астмы (12,13).
В этой клинической ситуации необходимо учитывать наличие эпидемиологических предпосылок коклюша, нарастающий характер кашлевых приступов. Характерны для коклюша репризы в приступах кашля, стекловидный характер мокроты, полная неэффективность β2-агонистов и глюкокортикостероидов. Окончательную ясность вносят бактериологический и серологический анализы. Важно заподозрить инфекционное заболевание в самом его начале, что может предотвратить распространение инфекции.
В последние годы, благодаря эффективному лечению значительно продлевается жизнь больных с муковисцидозом. Эту патологию может встретить в своей практике уже не только педиатр, но и терапевт. В этом случае возникают дифференциально диагностические трудности. Муковисцидоз - системное наследственное заболевание, при котором поражаются экзокринные железы. Причиной муковисцидоза является генная мутация, передающаяся по аутосомно – рецессивному типу. 1 из 2500 новорожденных в Северной Европе носит в себе ген муковисцидоза (14). Более 1500 вариантов мутаций гена трансмембранного регулятора хлоридных каналов клеток экзокринных желез обусловливают разнообразие клинической картины заболевания. Иногда болезнь протекает настолько скрыто, что о природе заболевания узнают, только когда ребенок становиться взрослым.
В клинической картине муковисцидоза превалируют симптомы хронического рецидивирующего воспаления дыхательных путей, сопровождающегося непродуктивным кашлем, одышкой, разнообразными хрипами в легких. При исследовании ФВД обнаруживаются симптомы бронхиальной обструкции, которые могут уменьшаться под воздействием β2-агониста. Иногда муковисцидоз протекает совместно с бронхиальной астмой. У таких больных обнаруживают сенсибилизацию к экзоаллергенам. Если 7 -дневный курс глюкокортикостероидной терапии (2мг/кг в сутки) не привел к купированию воспалительного процесса в трахеобронхиальном дереве, необходимо думать о наличие у больного муковисцидоза и проводить потовую пробу. Особенно, если имеются признаки мал абсорбции. Концентрация хлоридов в потовой жидкости <40 mEq/L является основанием для исключения муковисцидоза из списка причин хронического воспаления бронхов у данного пациента. Уровень хлоридов от 40 до 60 mEq/L должен побуждать врача к проведению генетического анализа для выявления наличия 2 мутаций гена трансмембранной регуляции, так как встречаются мутации, при которых болезнь протекает с менее выраженными симптомами и умеренным повышением уровня хлоридов в потовой жидкости (15).
Больные некоторыми, не часто встречающимися заболеваниями верхних дыхательных путей, иногда длительно наблюдаются с диагнозом бронхиальная астма, так как заболевание у них сопровождается кашлем одышкой и даже приступами удушья. Например, патологическая аддукция голосовых связок во время вдоха может привести к удушью, которое расценивается врачом как проявление бронхоспазма (16). В этой ситуации, в отличие от бронхиальной астмы, не эффективны ингаляции β2-агониста, а удушье носит характер стридора, то есть одышки инспираторного характера. Если провести исследование кривой «поток – объем», то мы получим овальную форму кривой маневра форсированного вдоха и выдоха, на графике – будут резко снижены показатели скоростных характеристик дыхания (17). Патологические движения голосовых связок при их дисфункции можно увидеть при ларингоскопии.
Дисфункция голосовых связок нередко возникает и как осложнение бронхиальной астмы (18), в этих случаях, как правило, имеются сопутствующие симптомы выраженного нервного возбуждения, беспокойства. Терапия внушением и самовнушением часто прекращает приступ одышки, если удается успокоить больного.
Иногда хронический кашель, а также одышку при физической нагрузке, наличие сухих хрипов в легких у больных, страдающих врожденной бронхоэктатической болезнью или синдромом Картагенера принимаются за проявления бронхиальной астмы. Ошибочность диагноза становится очевидной после безуспешных попыток лечить заболевание глюкокортикостероидами и β2-агонистами. Напротив, антибактериальная терапия высокоэффективна при купировании обострений легочного заболевания. Выявление правостороннего расположения сердца в грудной клетке, а также наличие патологии реснитчатого аппарата слизистой дыхательных путей позволяют уверенно диагностировать синдром Картагенера. Уже при первичном осмотре можно заподозрить врожденную аномалию: задержка роста, полидактилия, агенезия или гипогенезия лобных пазух, полипоз носа, пороки развития позвонков и ребер, мочевыводящих путей, концевые фаланги пальцев в виде «барабанных палочек», - все это может сопровождать дыхательные расстройства у больных с первичной цилиарной дискинезией.
Для дифференциальной диагностики врожденной бронхоэктатической болезни и бронхиальной астмы, особенно, в тех случаях, когда имеются «сухие» бронхоэктазы и нет обильной трехслойной мокроты, окончательно диагноз подтверждается бронхографически. При исследовании ФВД у больного с синдромом Картагенера можно обнаружить признаки бронхиальной обструкции, но отсутствие ТБГР и ТБГЧ позволяют клиницисту избежать гипердиагностики бронхиальной астмы.
Избыточная ригидность хрящевого каркаса трахеи и главных бронхов (трехеомаляция) может стать причиной повышения внутригрудного давления при кашле и резком выдохе и, как следствие, одышки. При этом, передняя и задняя стенки трахеи и главных бронхов соприкасаются, провоцируя непродуктивный кашель, формируя препятствие, как для выдоха, так и вдоха (19). Естественно, что в этой ситуации ингаляции β2-агониста могут только усугубить одышку и кашель. Необходимо осуществить трахео-бронхоскопию, она подтвердит диагноз заболевания хрящевой мембраны трахеи и главных бронхов. В тяжелых случаях проводится операция аортопексия, позволяющая отделить аорту от стенки трахеи (20).
В противоположность трехеомаляции, западение мягкой части стенки трахеи также способно стать причиной падения максимального потока форсированного выдоха. Такие пациенты начинают резко задыхаться в положении «лежа» и вынуждены вскакивать от удушья, только прикоснувшись затылком к подушке. Иногда помогает попытка выдохнуть через сомкнутые губы или через «соломинку». Создавая область повышенного давления в трахее, с усилием выдыхая через сомкнутые губы, удается вправить выпавшую мягкую ткань в стенку трахеи и открыть воздухоносные пути. Описаны ситуации, когда трахеобронхиальная дискинезия провоцирует нарушение дыхания при физической нагрузке, имитируя астму физического усилия. В данной ситуации совершенно не эффективны ингаляции топических глюкокортикостероидов и β2-агонистов. Купирует диспноэ дыхательная гимнастика в условиях нервно-физической релаксации. Ларингоскопия дает возможность отличить ларингомаляцию от дисфункции голосовых связок, которая также способна вызвать удушье при физической нагрузке.
Встречаются клинические случаи, когда длительное время проводится глюкокортикостероидная и бронхолитическая терапия больным с инородным телом бронха. Как правило, такая «бронхиальная астма» относится к категории трудно поддающегося терапии заболевания. Высокие дозы стероидов не способны предотвратить рецидивы бронхоспазма, которые прекращаются сразу после бронхоскопического извлечения проросшего арбузного семечка или рыбной кости.
Роль инородного тела может сыграть медленно развивающийся центральный рак бронха. Такие больные годами лечатся от бронхиальной астмы, вплоть до появления массивных легочных ателектазов или экссудативного плеврита. Как правило, прием β2-агониста или топического стероида на некоторое время приносит облегчение, но болезнь продолжает неуклонно прогрессировать и эффективность противовоспалительной и бронхорасширяющей терапии постепенно снижается.
Выражение, что «кашель – это не всегда астма» подтверждается у пациентов с «привычным кашлем» (21). Грубый, часто повторяющийся, продолжающийся часами, никогда не возникающий во время сна кашель – чрезвычайно мучителен для больного и окружающих его людей. Проведение функциональных проб, рентгенологическое и бронхоскопическое исследования, как и терапия противоастматическими средствами, не дают никакого результата. Часто этот синдром возникает у больных, перенесших психоэмоциональную травму и легко поддается терапии внушением (22).
В литературе встречается описание и других редких случаев синдрома навязчивого кашля, который много лет врачи пытались лечить как бронхиальную астму (23).
Встречаются ситуации, когда гипертрофированная глоточная миндалина касается надгортанника и вызывает при этом кашлевой рефлекс. Только тонзилэктомия полностью прекращает кашель у больного.
Сложную диагностическую задачу ставят перед врачом, встречающиеся в клинической практике случаи сочетания хронического кашля и гастроэзофагального рефлюкса (24, 25).
Как правило, таких пациентов направляют к пульмонологу или аллергологу с целью исключить или подтвердить наличие бронхиальной астмы. В литературе обсуждается вероятность совместного сосуществованиея этих двух нозологических категорий (26), но чаще больные с гастроэзофагальным рефлюксом рефрактерны к терапии β2-агонистами и топическими стероидами. У них отсутствуют симптомы трахеобронхиальной гиперчувствительности и гиперреактивности. Дальнейшего изучения заслуживает вопрос влияния друг на друга бронхиальной астмы и гастроэзофагального рефлюкса (27).
Наличие жалоб на одышку и кашель у больного с болезнью Пиквика нередко склоняют клинициста к попытке вести данного больного как пациента с ХОБЛ или бронхиальной астмой.
Неудачное назначение β2-агонистов и глюкокортикостероидных препаратов, отсутствие обратимости бронхиальной обструкции, а также то, что соотношение ОФВ1 к ФЖЕЛ у больных с болезнью Пиквика - более 0,7 заставляет врача пересмотреть первичный диагноз. Тем более, что при у болезни Пиквика наблюдается очень характерная клиническая картина - избыточный и постоянно нарастающий вес, ночные апноэ, дневная сонливость, храп. Данная категория больных нуждается в специфическом, нередко хирургическом лечении, промедление, с назначением которого может привести к фатальному результату, поэтому в этой ситуации очень важно правильно определить характер заболевания.
При решении вопроса о нозологической природе кашля и одышки необходимо тщательно анализировать данные анамнеза жизни и профессиональной деятельности больного. Приэтом можно обнаружить в истории жизни пациента факт многолетнего пребывания в условиях запыленности. Например, если перед клиницистом находится больной, который длительное время работал в литейном цехе или на ткацком производстве, тогда, прежде всего, необходимо исключить наличие хронического пылевого бронхита или пневмокониоза, особенно важна ранняя диагностика наиболее тяжелой формы пневмокониоза – силикоза.
Главным в диагностике силикоза является рентгенологическое исследование. В самом начале заболевания на рентгенограммах появляются усиление и деформация легочного рисунка, ячеистость и сетчатость, возникают единичные тени силикотических узлов, уплотнение междолевой плевры. Изменения, как правило, симметричны, иногда более выражены в правом легком с преимущественной локализацией в средних и нижних отделах. В дальнейшем, формируется картина «снежной бури»: многочисленные мелкопятнистые неправильной формы тени с располагающимися между ними силикотическими узелками округлой формы, имеющие четкие контуры — II стадия заболевания. Далее, тени сливаются в крупные опухолевидные конгломераты с образованием в некоторых случаях полостей, чаще при сочетании с туберкулезом; выражены признаки эмфиземы легких – ΙΙΙ стадия. При проведении исследования ФВД можно обнаружить рестриктивные нарушения вентиляции, то есть показатели жизненной емкости легких (ЖЕЛ) снижаются, но при осложненном течении пневмокониоза могут появляться признаки бронхиальной обструкции и или трахеобронхиальной гиперреактивности, что свидетельствует о совместном существовании у больного профессионального заболевания легких и ХОБЛ или бронхиальной астмы.
Снижение ЖЕЛ в сочетании с резким увеличением скоростных показателей кривой «поток-объем» при исследовании ФВД позволяют заподозрить наличие у больного интерстициального поражения легких. При этом сопротивление дыханию будет падать, а признаки ТБГР и ТБГЧ не выявляются. В легких, при выслушивании, вместо сухих свистящих хрипов обнаруживается крепитация. Картина «сотового» легкого при рентгенографии позволяет клиницисту четко дифференцировать интерстициальную пневмонию от бронхиальной астмы.
При экзогенном альвеолите одновременно с рестриктивными нарушениями вентиляции могут присутствовать признаки бронхиальной обструкции – падение скорости форсированного выдоха на разных участках дыхательных путей. Признаки бронхиальной обструкции вместе с наличием эозинофилии в мокроте и крови, а также связь обострения заболевания с пребыванием в помещении, где содержатся животные или складируется зерно – все это позволяет дифференцировать бронхиальную астму у больного от экзогенного альвеолита. Эти два заболевания имеют существенные различия. Клиническая картина экзогенного альвеолита не характеризуется наличием эпизодов приступов удушья, механизм одышки при нем связан с отеком интерстициальной ткани легких. При экзогенном альвеолите имеются признаки интоксикации: субфебрильная температура тела, слабость, ломота в мышцах, головные боли, возникающие через 6 – 9 часов после контакта с термофильными актиномицетами или органической пылью, что совершенно не характерно для бронхиальной астмы. При исследовании ФВД, при экзогенном альвеолите, в отличие от бронхиальной астмы, нет признаков трахеоброхиальной гиперреактивности и гиперчувствительности, а при рентгенографии выявляются инфильтративные изменения легочных полей. На рентгенограммах легких, при экзогенном альвеолите, отмечается нечеткость легочного рисунка с обеих сторон, более выраженная в прикорневых и базальных отделах, на фоне которой определяются двусторонние мелкие очаговые тени с убывающей интенсивностью по направлению к верхушкам.
Причиной возникновения одышки и удушья может быть туберкулезная интоксикация (28). Важную роль в иммунитете к микобактерии играют аллергические реакции, способствующие формированию трахеобронхиальной гиперрективности – патогенетической основы бронхиальной астмы. Когда у больного имеются выраженная одышка и другие проявления бронхоспазма на второй план могут отступать симптомы туберкулеза, что способствует диагностической ошибке и гипердиагностике бронхиальной астмы на раннем этапе туберкулезного процесса.
В заключение, приводим несколько клинических примеров ошибочной диагностики бронхиальной астмы.
Больной Г. Длительнее время наблюдался с диагнозом бронхиальной астмы, осложненной эозинофильной пневмонией.
Жалобы на одышку при минимальной физической нагрузке, приступы удушья, купируемые ингаляцией вентолина, кашель, слабость, головную боль, периодически лихорадку до 38 градусов, боли в грудной клетке, боли в мышцах, суставах, резкое похудание (до 30 кг в течение 6 месяцев) слабость в ногах, потерю чувствительности в стопах.
Болен около полугода. Лечился в нескольких крупных стационарах Москвы, получал инфузионную терапию глюкокортикостероидами и бронхорасширяющими препаратами с временным улучшением. Длительная антибактериальная терапия различными группами препаратов приводила к ухудшению состояния пациента.
При поступлении: состояние больного тяжелое, резкая гипотрофия. В легких выслушивались сухие низкотональные хрипы. Тоны сердца приглушены, ритм правильный, граница сердца не расширены.
Ультразвуковое исследование сердца и внутренних органов не выявило значительных патологических изменений. При колоноскопии и компьютерной томографии онкологическое заболевание не обнаружено. Данные рентенографии грудной клетки на рис.1.
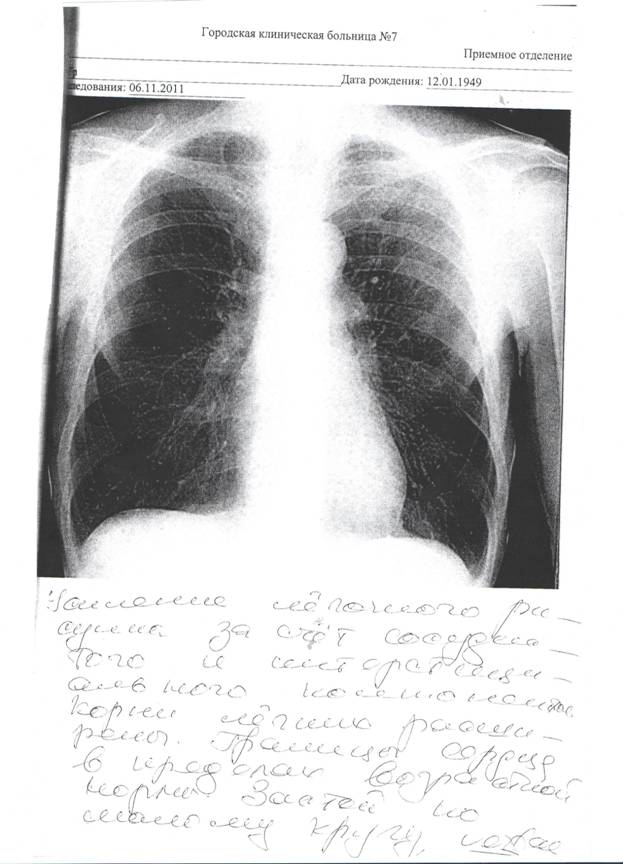
Рисунок 1 Рентгенограмма больного Г.
При исследовании ФВД, исходно диагностирована генерализованная бронхообструкция. После ингаляции албутерола – обратимость обструкции оказалась не полной, что не характерно для бронхиальной астмы, а соотношение ОФВ1 к ФЖЕЛ (в отчете – FEV1/FVC) – 0,75, что исключает диагноз ХОБЛ. Результаты – представлены на рисунке 2.
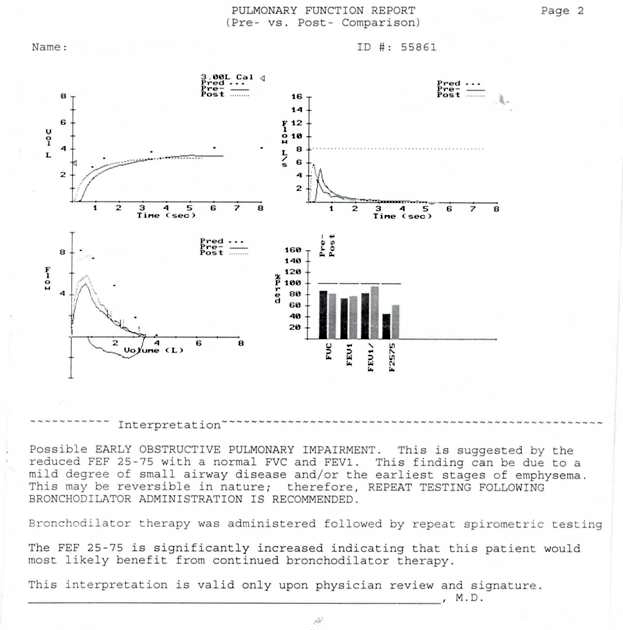
Рис. 2 Кривые «объем-время», «поток-время», «поток-время» и графическое изображение изменений основных показателей кривой «поток-объем» форсированного выдоха, до и после ингаляции 400 мкг вентолина.
Исследование проведено на спироанализаторе системы «КоКо». Анализируя полученные кривые, можно убедиться, что у больного имеется легкая степень обратимой обструкции.
Изменения показателей кривой «поток-объем» форсированного выдоха представлены на рис. 3.
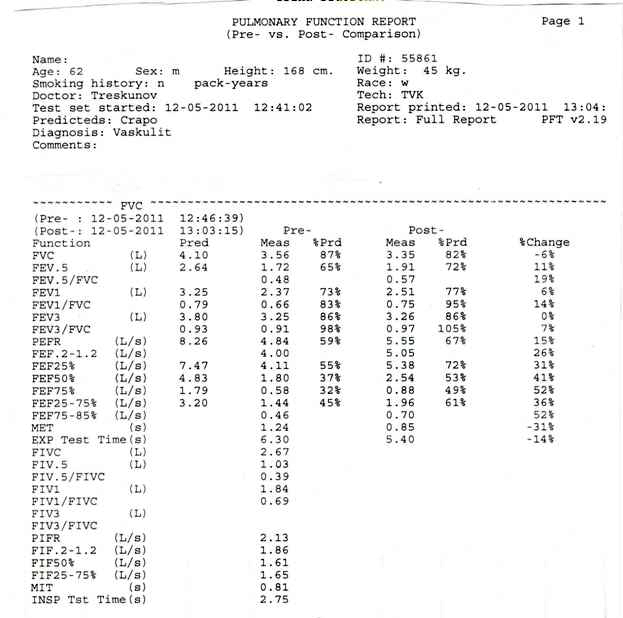
Рис.3 Распечатка результатов исследования ФВД до и после ингаляции вентолина.
FVC – ФЖЕЛ
FEV1 –ОФВ1
FEF25,50,75 - Максимальный поток форсированного выдоха на уровне 25, 50 и 75% ФЖЕЛ.
В анализе периферической крови были обнаружены множественные изменения – рис. 4. Анализ периферической крови.
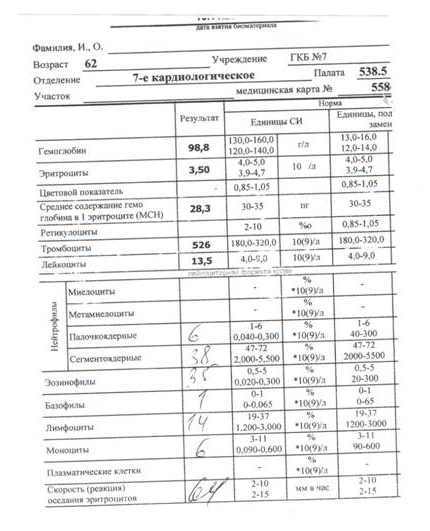
Обращали на себя внимание:
- Высокий уровень эозинофилии.
- Анемия.
- Проявления воспалительной реакции: лейкоцитоз, высокие цифры СОЭ.
Невропатологом был диагностирован множественный неврит нижних конечностей. В моче отмечались проявления поражения сосудистой части нефрона: белок, выщелоченные эритроциты и восковые цилиндры.
Таким образом, в клинической картине заболевания обращала на себя внимание системность поражения внутренних органов. Воспалительный процесс имел явный аутоиммунный патогенез и затрагивал респираторную систему. Заболевание, что характерно, началось с приступов удушья, что заставило на раннем этапе диагностировать бронхиальную астму. Как оказалось, имеющийся бронхоспазм носил синдромный характер. Анализируя клиническую картину, характер течения патологического процесса, данные обследования, был поставлен диагноз узелкового периартериита. Назначение 60 мг преднизолона в сутки внутрь позволило через 14 дней полностью купировать проявления заболевания. Больной был выписан на поддерживающей дозе глюкокортикостероида под наблюдение ревматолога.
Подводя итог, необходимо отметить, что диагноз бронхиальной астмы нередко остается трудной задачей для практического врача. В диагностическом процессе необходимо опираться на существующее определение заболевания разработанное Комитетом Экспертов, в котором центральное место занимает обратимая бронхообструкция, трахеобронхиальная гиперчувствительность и гиперреактивность. Поэтому уже при опросе больного необходимо обратить внимание на характерные для бронхиальной астмы симптомы: кашель и одышка, возникающие при резкой смене температуры и влажности вдыхаемого воздуха, а также при глубоком и частом дыхании, появление одышки в период отдыха от кратковременной и интенсивной физической нагрузки. При расспросе больного очень важно выяснить реакцию его на прием медикаментов с -адреноблокирующими свойствами, блокаторов ангиотензинпревращающего фермента. Нередко, у пожилого пациента трудно купируемая одышку при наличие бронхиальной астмы можно объяснить приемом бисопролола, пропранолола или эналаприла. Данные о провоцирующем кашель и одышку действии различных экзоаллергенов (домашняя пыль, эпидермис животных, пыльца растений), медикаментов, например, аспирина, так же направляют мысль врача в сторону наличия у больного бронхиальной астмы. Решающее значение для дифференциальной диагностики, например, ХОБЛ и бронхиальная астма, имеет время начала симптомов заболевания. Если кашель и одышка появились до 40 летнего возраста, диагноз ХОБЛ становится сомнительным. Очень информативным может стать тщательно собранный семейный анамнез. Как правило, при тщательном расспросе можно обнаружить у больного бронхиальной астмой кровных родственников, страдающих поллинозом, одним из видов аллергии или также как и сибс - бронхиальной астмой.
При объективном обследовании больного с подозрением на бронхиальную астму обращает на себя внимание наличие высоко тональных сухих хрипов, выслушиваемых при аускультации легких, провоцируемых глубоким вдохом и резким выдохом, и исчезающих через 10 минут после ингаляции албутерола. Характерен цвет мокроты – часто у больного бронхиальной астмой она окрашена в оранжевый из-за наличия эозинофилов и продуктов их распада цвет.
Наконец, чтобы подтвердить диагноз бронхиальной астмы, врач должен назначить больному исследование ФВД с обязательной фармакологической пробой на обратимость обструкции бронхов даже, если она «скрытая», то есть, когда результаты измерения укладываются в существующие стандарты. После ингаляции албутерола можно получить значительный прирост ОФВ1 . В сложных диагностических случаях появляется потребность в проведение бронхоконстрикторного теста.
И последнее, необходимо иметь в виду, что каждый больной имеет право обладать сразу несколькими заболеваниями, которые могут оказывать влияние друг на друга и вызывать схожие симптомы. Спорным остается вопрос о правомерности диагностики у одного больного одновременно двух заболеваний: бронхиальной астмы и ХОБЛ, что нередко встречается в анализируемых историях болезни. Если исходить из определения бронхиальной астмы и ХОБЛ, данного Комитетом Экспертов, подобный симбиоз невозможен и диагноз – ХОБЛ+Астма вносит путаницу в формирование тактики ведения больного.
Список литературы
- Под ред. Чучалина А.Г. Глобальная стратегия лечения и профилактики бронхиальной астмы. — М: «Атмосфера», 2007. — С. 104.
- Global Initiative for Asthma — 2006. — 106 с.
- Овчаренко С. И. Бронхиальная астма: диагностика и лечение. — РМЖ, 2002. — Т. 10. — № 17.
- Цитировано по кн. «Клиническая аллергология и иммунология». Руководство для практикующих врачей. Под редакцией Л.А. Горячкиной, К.П. Кашкина. Москва. Миклош. 2009. Стр. 135.
- Boulet L.P., Turcotte H., Carrier G., Boulet M., Laviolette M.: Increased maximal airway response to methacholine during seasonal allergic rhinitis in nonasthmatic subjects; relationships with airway wall thickness and inflammation. Eur. Respir.J. 8:913. 1995.
- van Haren E.H., Lammers J.W., Festen J., van Herwaarden C.L.: Bronchial vagal tone and responsiveness to hisiamine, exercise and bronchodilatators in adult patients with cystic fibrosis. Eur. Resp. J. 5: 1083, 1992.
- Ramsdale E.H., Morris M.M., Roberts R.S., Hargreave F.E.: Bronchial responsiveness to methacholine in chronic bronchitis: relationship to airflow obstruction and cold air responsiveness. Thorax 39:912. 1984.
- Global initiative for chronic Obstructive Lung Disease. Updated December 2007. Available from; www.goldcopd.com.
- Standardisation of spirometry Miller M.R. et all. Eur. Respir.J. 2005. 26; 319-338.
- A. Calderón-Larrañaga, L. Carney, M. Soljak, A. Bottle,M. Partridge, D. Bell, G. Abi-Aad, P. Aylin, A. Majeed.Thorax 2011;66:191-196 doi:10.1136/thx.2010.147058.
- Thomson F, Masters IB, Chang AB. Persistent cough in children and the overuse of medications. J Paediatr Child Health.2002;38 :578– 581.
- Wright SW, Edwards KM, Decker MD, Zeldin MH. Pertussis infection in adults with persistent cough. JAMA.1995;273 :1044– 1046. Mink CM, Cherry JD, Christenson P, et al. A search for Bordetella pertussis infection in university students. Clin Infect Dis.1992;14 :464– 471.
- Gilljam M, Ellis L, Corey M, Zielenski J, Durie P, Tullis DE. Clinical manifestations of cystic fibrosis among patients with diagnosis in adulthood. Chest.2004; 126:1215– 1224.
- Gilljam M, Ellis L, Corey M, Zielenski J, Durie P, Tullis DE. Clinical manifestations of cystic fibrosis among patients with diagnosis in adulthood. Chest.2004;126 :1215– 1224.
- Christopher KL, Wood RP 2nd, Eckert RC, Blager FB, Raney RA, Souhrada JF. Vocal-cord dysfunction presenting as asthma. N Engl J Med.1983;308 :1566– 1570.
- M.Weinberger When Asthma is Not Asthma. Clinical Pulmonary Medicine 2011; 18(5): 207-14. Doshi D. Weinberger M. Long-term outcome of vocal cord dysfunction. Ann Allergy Asthma Immunol 2006;96;794-799.
- RE Wood. Localized tracheomalacia or bronchomalacia in children with intractable cough. J Pediatr.1990;116 :404– 406.
- Doshi DR, Weinberger MM. Long-term outcome of vocal cord dysfunction. Ann Allergy Asthma Immunol.2006;96 :794– 799
- TR Weber, MS Keller, A Fiore. Aortic suspension (aortopexy) for severe tracheomalacia in infants and children. Am J Surg.2002;184 :573– 577.
- B. Lokshin, S. Lindgren, M. Weinberger, J. Koviach. Outcome of habit cough in children treated with a brief session of suggestion therapy. Ann Allergy.1991;67 :579– 582.
- Ran D. Anbar, Pseudo-asthma Revisited Pediatrics Vol. 121 No. 1 January 1, 2008 pp.221 (doi: 10.1542/peds.2007-3045)
- Weinberger, MD, M. Abu-Hasan. Pseudo-asthma: When Cough, Wheezing, and Dyspnea Are Not Asthma. Pediatrics Vol. 120 No. 4 pp. 855 -864.October 1, 2007
- Najada A, Weinberger M. Unusual cause of chronic cough in a four-year-old cured by uvulectomy. Pediatr Pulmonol.2002;34 :144– 146.
- Weinberger M. Gastroesophageal reflux is not a significant cause of lung disease in children. Pediatr Pulmonol.2004;37(suppl 26) :194– 196.
- Chang AB, Lasserson TJ, Gaffney J, Connor FL, Garske LA. Gastro-oesophageal reflux treatment for prolonged non-specific cough in children and adults. Cochrane Database Syst Rev.2006;(4) : CD004823.
- Л.И. Дворецкий. Кашель: диагностический поиск. Consilium Medicum. Приложение.2001. Том 2. Стр.3-6.
- M. Cazzola, L.Cazetta, G. Bettonceli, L. Novelli, C. Gricelli, P. Rogliani. Asthma and comorbid medical illness. August 2011, Vol.8. No 4, 308-319.
- Vikram Khoshoo, MD, PhD, Dean Edell, MD, MPH, FCCP, Sopan Mohnot, Robert Haydel, Jr, MD, Emilio Saturno, MD and Aaron Kobernick, MD, Associated Factors in Children With Chronic Cough .CHEST September 2009 vol. 136 no. 3 811-815.